
技術(shù)文章
 更新時間:2025-09-16
更新時間:2025-09-16 點擊次數(shù):151
點擊次數(shù):151
蛋白質(zhì)降解技術(shù)(PROTAC)借助細(xì)胞內(nèi)天然的泛素-蛋白酶體系統(tǒng),實現(xiàn)目標(biāo)蛋白的特異性降解,已成為新藥研發(fā)領(lǐng)域的重要策略。然而,傳統(tǒng)PROTAC分子在體內(nèi)應(yīng)用中仍面臨脫靶毒性、組織非特異性分布以及由過度活化引起的非預(yù)期蛋白降解等問題,嚴(yán)重限制其臨床轉(zhuǎn)化潛力。
針對上述挑戰(zhàn),發(fā)表于《Journal of the American Chemical Society》的一項研究提出了一種新型“生物正交前藥"策略。該研究設(shè)計了一類基于逆電子需求狄爾斯-阿爾德(IEDDA)反應(yīng)的“點擊釋放型PROTAC前藥"(crPROTAC)。IEDDA反應(yīng)因其優(yōu)異的生物相容性、高速率常數(shù)和高正交性,特別適用于復(fù)雜生物環(huán)境中的靶向激活。
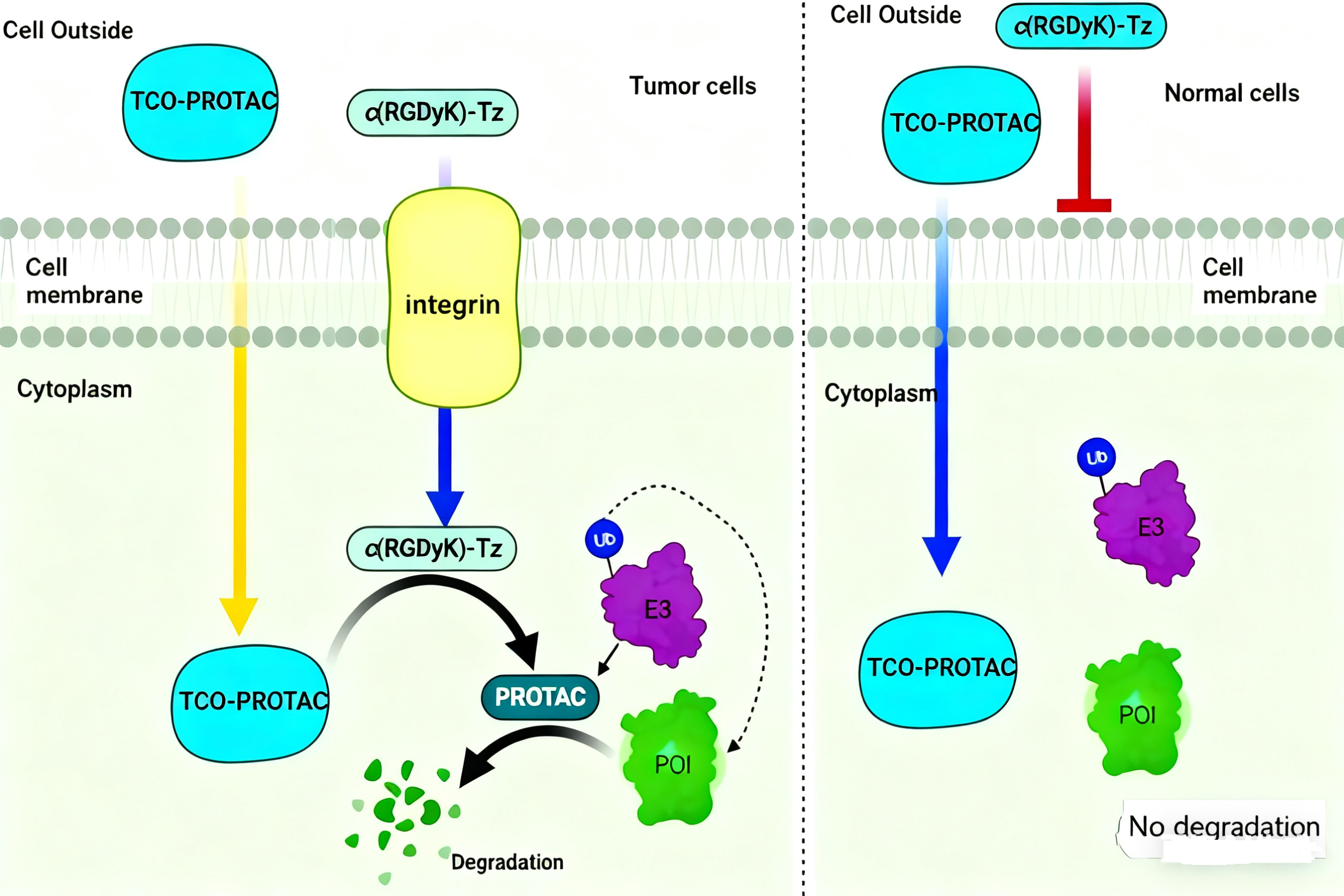
具體而言,研究團隊合成了兩種惰性前藥形式:TCO-ARV-771 和 TCO-DT2216。它們通過在PROTAC分子上引入反式環(huán)辛烯(TCO)保護(hù)基團,阻斷其與E3泛素連接酶及目標(biāo)蛋白的正常結(jié)合,從而避免在非靶區(qū)域激活。當(dāng)前藥與帶有疊氮苯并環(huán)辛炔(Tz)修飾的靶向配體——例如常用于腫瘤靶向的c(RGDyK)肽——相遇時,TCO與Tz發(fā)生IEDDA反應(yīng),原位釋放出具有活性的PROTAC分子,實現(xiàn)精準(zhǔn)的靶點激活和蛋白降解。
該策略不僅在細(xì)胞模型中顯著降低了脫靶降解,還提高了PROTAC在異種移植瘤模型中的抗腫瘤效果與安全性,為開發(fā)基于生物標(biāo)志物響應(yīng)型的下一代PROTAC前藥提供了堅實理論基礎(chǔ)和技術(shù)路徑。
E3泛素連接酶在調(diào)控蛋白質(zhì)穩(wěn)定性、信號轉(zhuǎn)導(dǎo)及細(xì)胞進(jìn)程等方面發(fā)揮核心作用,其功能異常與腫瘤、神經(jīng)退行性疾病等多種病理狀態(tài)密切相關(guān)。然而,由于缺乏實時、高效的酶活監(jiān)測工具,E3連接酶的研究及其抑制劑開發(fā)一直面臨較大困難。
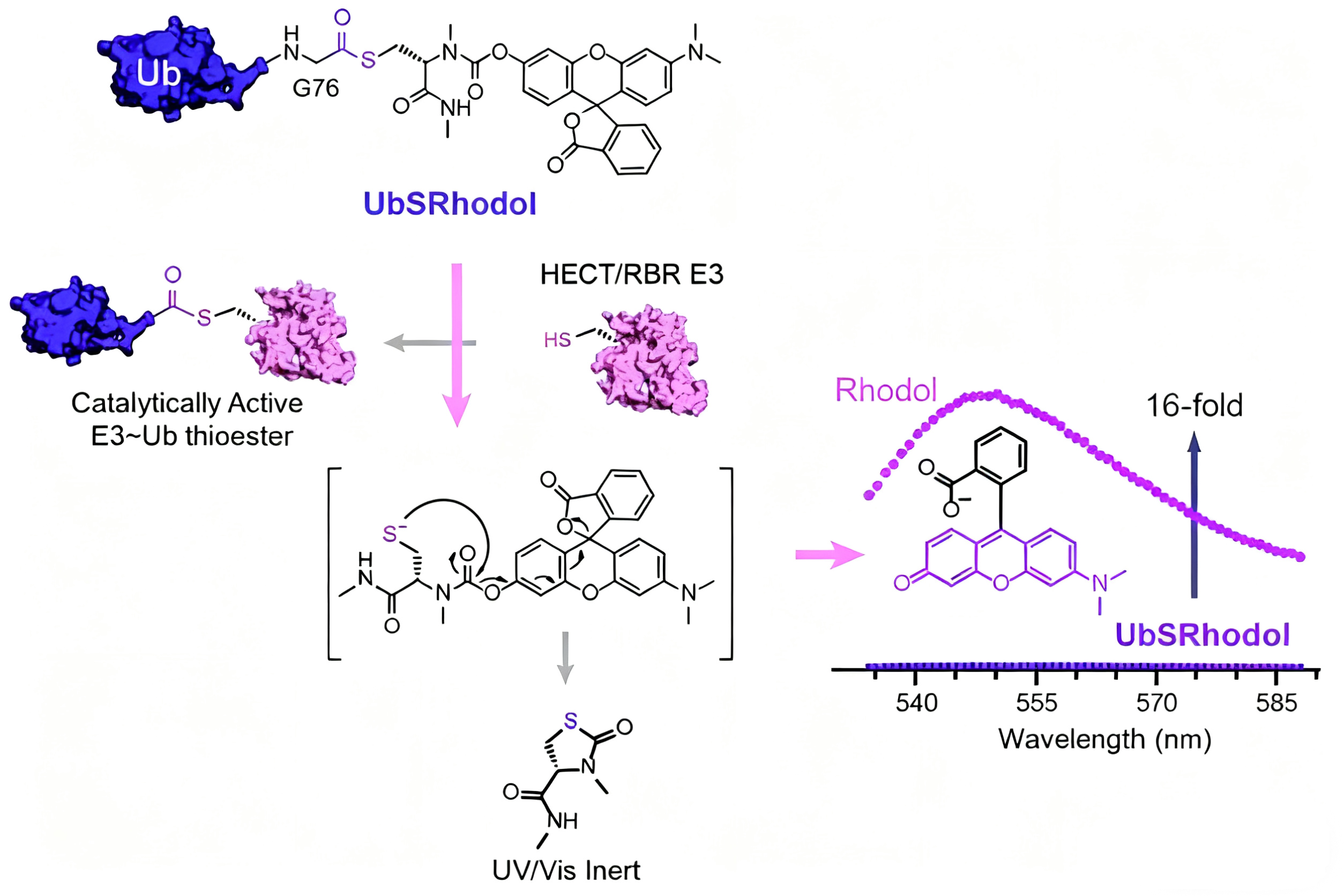
近期,《Angewandte Chemie International Edition》報道了一種開創(chuàng)性的遺傳編碼型前熒光探針——UbSRhodol,可用于實時、定量檢測依賴于半胱氨酸的E3連接酶活性。該探針巧妙地將泛素(Ub)的C端通過氨基甲酸酯鍵連接至掩蔽狀態(tài)的羅丹明熒光團,形成硫酯中間體模擬物。在自然狀態(tài)下,羅丹明以內(nèi)酯形式存在,幾乎無熒光;而當(dāng)E3連接酶催化半胱氨酸攻擊該硫酯鍵時,會發(fā)生轉(zhuǎn)硫酯化反應(yīng),生成E3~Ub共價復(fù)合物,并同時釋放出游離的羅丹明,恢復(fù)強烈熒光信號。
研究者驗證了UbSRhodol在多種E3酶(如Ube2T、Parkin等)活性檢測中的適用性,并展示了其應(yīng)用于高通量抑制劑篩選平臺的潛力。不僅如此,該探針還可用于監(jiān)測蛋白質(zhì)-蛋白質(zhì)相互作用引起的構(gòu)象變化及酶動力學(xué)過程,為理解泛素信號網(wǎng)絡(luò)的動態(tài)調(diào)控提供了新型化學(xué)工具。
這一技術(shù)不僅推動E3連接酶功能研究的深度和廣度,也為針對E3的藥物發(fā)現(xiàn)和化學(xué)生物學(xué)研究提供了強有力的手段。
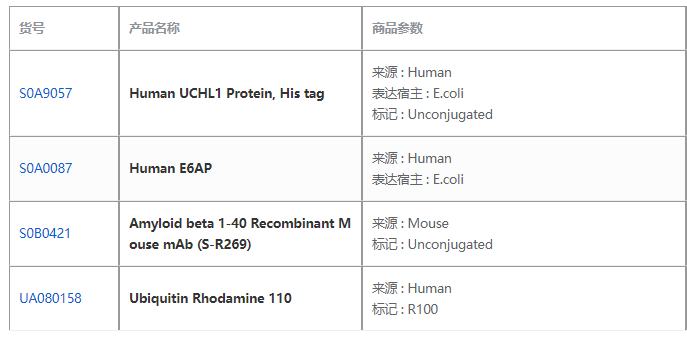
杭州斯達(dá)特 志在為全球生命科學(xué)行業(yè)提供優(yōu)質(zhì)的抗體、蛋白、試劑盒等產(chǎn)品及研發(fā)服務(wù)。依托多個開發(fā)平臺:重組兔單抗、重組鼠單抗、快速鼠單抗、重組蛋白開發(fā)平臺(E.coli,CHO,HEK293,InsectCells),已正式通過歐盟98/79/EC認(rèn)證、ISO9001認(rèn)證、ISO13485。
如何實現(xiàn)PROTAC前藥的靶向激活以提升治療特異性?
關(guān)注公眾號

Copyright © 2025杭州斯達(dá)特生物科技有限公司 All Rights Reserved 工信部備案號:
技術(shù)支持:化工儀器網(wǎng) 管理登錄 sitemap.xml