
技術文章
 更新時間:2025-09-22
更新時間:2025-09-22 點擊次數:161
點擊次數:161
成纖維細胞生長因子18(FGF18)是成纖維細胞生長因子(FGF)家族的成員之一,該家族由22個結構相關的信號蛋白組成,在哺乳動物中廣泛參與調控細胞增殖、分化、遷移和存活等一系列關鍵生物學過程。FGF18于1998年被發現并克隆,其基因位于人類染色體5q35.1。在系統進化上,FGF18與FGF8和FGF17共同歸屬于FGF8亞家族(也稱為旁分泌FGF亞家族),它們享有較高的氨基酸序列同源性,但在體內卻執行著獨特的功能。與主要通過內分泌方式作用于遠處靶器官的FGF19、FGF21和FGF23不同,FGF18屬于典型的旁分泌信號分子。這意味著它由細胞合成和分泌后,主要作用于鄰近的細胞,其活性受到與硫酸乙酰肝素蛋白聚糖(HSPG)結合的嚴格調控,這種結合對于FGF18與其受體形成穩定的三元復合物至關重要,從而限制了其作用范圍,確保了信號傳遞的精確性和局部性。FGF18通過特異性結合并激活細胞膜表面的FGF受體(FGFR),其中它與FGFR2c和FGFR3c兩種受體亞型的親和力最高。受體激活后,會啟動細胞內RAS/MAPK、PI3K/AKT、PLCγ和STAT等多條下游信號通路,最終將細胞外信號轉化為特定的細胞核內生物學應答,從而在胚胎發育、組織穩態和修復再生中扮演著指揮者的角色。
FGF18的表達具有顯著的時間和空間特異性,其功能貫穿于從胚胎期到成年期的多個階段,尤其在骨骼系統的發育和穩態維持中發揮著核心作用。在胚胎發育過程中,FGF18是骨骼形成(骨發生)的關鍵調控因子。它通過在軟骨內成骨過程中協調軟骨細胞的增殖、分化和凋亡,來精確調控骨骼的生長和模式構建。在生長板中,FGF18主要由周圍的骨膜細胞和肥大的軟骨細胞產生,它通過激活軟骨細胞上的FGFR3,強烈抑制軟骨細胞的增殖,同時促進其向肥大階段分化,并最終引導血管入侵和軟骨基質鈣化,為骨組織的替換做好準備。基因敲除研究清晰地揭示了FGF18的重要性:Fgf18缺陷的小鼠表現出嚴重的骨骼發育異常,包括長骨顯著縮短、胸骨融合缺陷、顱縫早閉以及肺泡發育不全等表型,這充分證明了FGF18對于正常骨骼模式形成和生長的重要性。
除了對骨骼系統的核心作用,FGF18在其他組織和器官中也扮演著多重角色。在中樞神經系統中,FGF18在胚胎大腦的特定區域(如皮層和海馬)表達,參與調控神經前體細胞的存活和分化,影響大腦的正常發育和回路形成。在肺部,它促進肺泡上皮細胞的增殖和分支形態發生,對肺臟的正常發育至關重要。在成年機體中,FGF18的表達水平雖有所下降,但并未沉默。它持續在骨骼、關節軟骨、肝臟和大腦等組織中低水平表達,參與維持組織的穩態。特別是在關節軟骨中,FGF18表現出獨特的雙重功能:一方面,它可以通過促進軟骨前體細胞的增殖和基質合成來發揮合成代謝作用;另一方面,在炎癥環境下,它也可能參與分解代謝過程。此外,越來越多的證據表明,FGF18在損傷修復和再生過程中被重新激活,例如在骨折愈合、肝部分切除后的肝再生以及肌肉損傷模型中,FGF18的表達顯著上調,提示它可能是組織響應損傷、啟動修復程序的一個重要信號分子。
FGF18信號的失調,無論是過度激活還是功能缺陷,都與多種人類疾病的病理過程密切相關,這使得它成為一個備受關注的疾病相關分子和潛在的治療靶點。在骨骼和關節疾病領域,FGF18-FGFR3信號軸的異常增強是軟骨發育不全(Achondroplasia)和-thanatophoric dysplasia(致死性發育不良)等骨骼發育障礙的主要病因。這些疾病通常由FGFR3的組成型激活突變引起,導致FGF18/FGFR3信號通路被持續、強烈地激活,從而過度抑制了生長板軟骨細胞的增殖,造成嚴重的肢體短縮和侏儒癥。另一方面,在骨關節炎(Osteoarthritis, OA) 中,關節軟骨的進行性退變是其核心特征。雖然骨關節炎的病理復雜,但FGF信號網絡在其中扮演著矛盾的角色。有研究表明,在骨關節炎的關節中,FGF18及其受體的表達模式發生改變,其信號平衡被打破,可能參與了軟骨降解的進程。然而,令人感興趣的是,外源性補充重組的FGF18蛋白卻又被證明能夠刺激軟骨細胞的增殖和細胞外基質(如蛋白聚糖和II型膠原)的合成,顯示出強大的軟骨保護潛力,這凸顯了FGF18信號在關節健康與疾病中復雜且情境依賴性的功能。
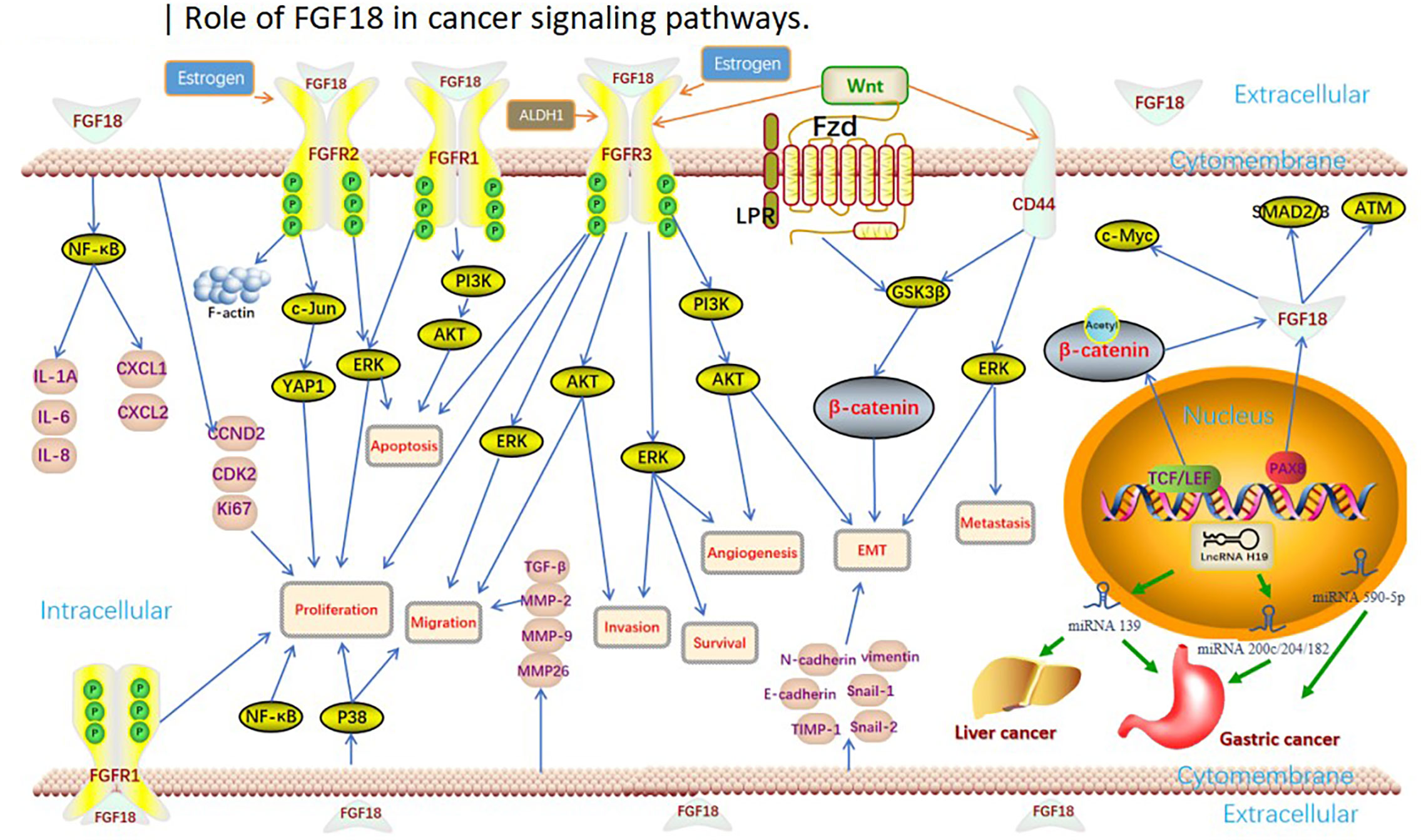
beyond骨骼系統,FGF18的異常表達也與腫瘤的發生和發展聯系在一起。多項研究發現在肝細胞癌、結直腸癌、非小細胞肺癌和前列腺癌等多種實體瘤中,FGF18的表達水平顯著高于癌旁正常組織。FGF18通過其促有絲分裂、促血管生成和抗凋亡的特性,以自分泌或旁分泌的方式為腫瘤細胞的惡性增殖和存活提供生長優勢。例如,在肝細胞癌中,高表達的FGF18通過激活FGFR4和下游的ERK信號通路,驅動腫瘤細胞增殖并抑制其凋亡,與較差的臨床預后相關。此外,FGF18還能刺激腫瘤基質中新生血管的形成,為快速生長的腫瘤提供充足的氧氣和營養。因此,靶向FGF18/FGFR信號軸已成為癌癥治療領域一個新興的探索方向,針對該通路的單克隆抗體和小分子抑制劑正在臨床前和臨床研究中接受評估,以期切斷這條驅動腫瘤生長的關鍵信號線路。
鑒于FGF18在促進組織修復和再生方面的強大潛能,將其開發為治療性藥物,特別是用于治療肌肉骨骼系統損傷和退行性疾病,成為了生物醫藥產業的一個熱點。目前,最令人矚目的進展集中在其對骨關節炎的治療應用。重組人FGF18(如Sprifermin)作為一種局部給藥的生物制劑,已在臨床前模型和人體臨床試驗中展示了巨大的前景。在動物模型中,關節腔內注射Frifermin能夠顯著刺激關節軟骨的再生和增厚,增加軟骨基質成分的合成,并減緩軟骨缺損的進展。隨后進行的多項隨機、雙盲、安慰劑對照的II期臨床試驗結果表明,與安慰劑相比,每年兩次關節內注射Sprifermin,能夠顯著且持續地增加膝關節股骨髁的軟骨厚度,表明其確實具有改變疾病進程的能力(Disease-Modifying Osteoarthritis Drug, DMOAD的潛力)。雖然其在緩解疼痛癥狀方面的效果不一,但其促進軟骨再生的能力為從根本上治療骨關節炎帶來了希望。目前,更大規模的III期臨床試驗正在籌備或進行中,以進一步驗證其長期療效和安全性。
除了骨關節炎,FGF18在骨折愈合和軟骨修復領域也展現出治療價值。臨床前研究顯示,局部應用FGF18可以加速骨折愈合過程,促進骨痂形成和骨改建,改善愈合骨的質量,這對于治療延遲愈合或不愈合骨折具有重要的臨床意義。在牙周組織再生方面,FGF18也被探索用于促進牙槽骨和牙周韌帶的再生。展望未來,FGF18的治療應用可能將進一步拓展。其在神經保護、肝再生等方面的基礎研究功能提示,它未來或可用于治療神經系統損傷、神經退行性疾病以及促進肝臟手術后的功能恢復。然而,將FGF18成功轉化為廣泛應用的藥物仍面臨諸多挑戰。其固有的肝素結合特性可能導致其在注射部位滯留,并可能引發潛在的脫靶效應。精確控制其給藥劑量、頻率和遞送方式至關重要,以其合成代謝益處,同時最小化其可能促進異常增生或腫瘤生長的理論風險。此外,開發更穩定、更具靶向性的FGF18變體或類似物,以及將其與先進的生物材料支架結合以實現局部持續釋放,將是未來研究的重要方向。
成纖維細胞生長因子18(FGF18)是一個多功能的信號蛋白,其生物學功能遠不止于其名字所暗示的范圍。從指揮胚胎骨骼的精密構建,到維持成年組織的穩態,再到響應損傷并啟動修復程序,FGF18的作用貫穿生命始終。它既是在正確時空背景下維持健康的關鍵衛士,其信號通路的失調也是多種疾病(從骨骼畸形到癌癥)的驅動因素。這種功能上的雙重性,既帶來了挑戰,也提供了巨大的機遇:一方面,我們需要更深入地理解其復雜且情境依賴性的信號調控機制;另一方面,它為我們開發針對骨關節炎、骨折不愈合乃至某些癌癥的創新療法提供了一個強有力的分子工具。未來的研究將更加側重于解析FGF18在不同組織微環境中的精確作用機制,開發新一代更安全、更高效的治療策略(如組織靶向性遞送、功能優化蛋白變體、與生物材料結合等),并積極探索其在神經再生、心血管疾病等新領域的應用潛力。隨著基礎科學和轉化研究的不斷深入,FGF18有望從一個重要的基礎生物學分子,蛻變為真正造福患者的革命性治療藥物,為再生醫學和治療學開啟新的篇章。
杭州斯達特 志在為全球生命科學行業提供優質的抗體、蛋白、試劑盒等產品及研發服務。依托多個開發平臺:重組兔單抗、重組鼠單抗、快速鼠單抗、重組蛋白開發平臺(E.coli,CHO,HEK293,InsectCells),已正式通過歐盟98/79/EC認證、ISO9001認證、ISO13485。
成纖維細胞生長因子18(FGF18):從發育調控到治療新星的多面角色